突破性进展|CS-PEI包裹circRNA纳米疫苗,为禽用抗病毒疫苗开辟新路径
审核人:刘马峰 编辑:田斌
近日,我校程安春教授团队田斌副教授课题组在新型鸭呼肠孤(NDRV)核酸纳米颗粒疫苗研发领域取得重要进展。相关成果以“Nanovaccine based on Chitosan Oligosaccharide-Polyethyleneimine packaged circRNA Encoding Sigma C Proteins Elicits Protective Immunity against Novel Duck Reovirus in Ducks”为题,在线发表于国际学术期刊《International Journal of Biological Macromolecules》,为新型鸭呼肠孤高效防控供了创新技术方案。

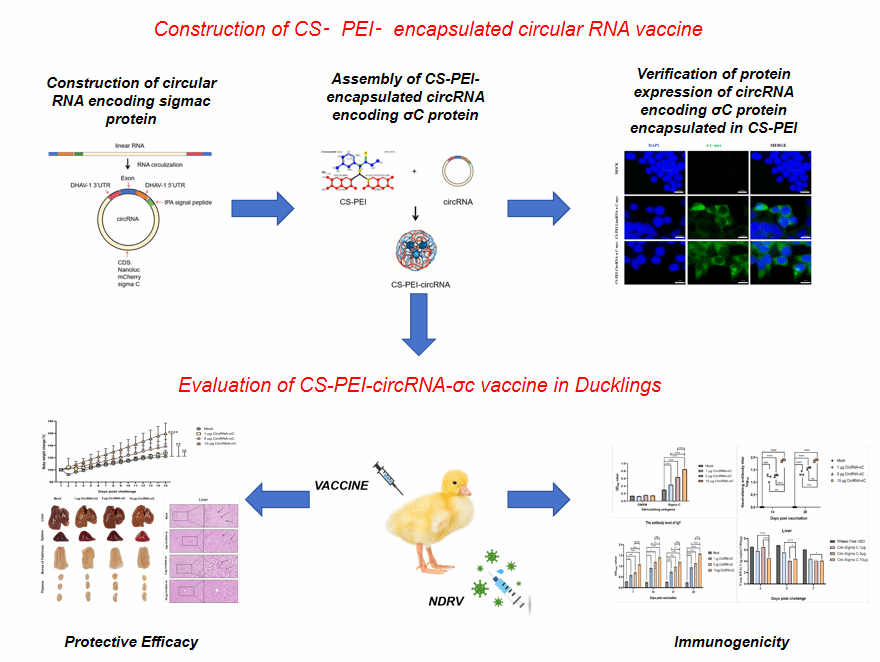
在畜禽养殖业规模化发展的今天,病毒性疾病始终是制约行业高质量发展的关键瓶颈,其中新型鸭呼肠孤病毒(NDRV)引发的鸭出血性坏死性肝炎,以高传染性、高死亡率的特点,严重威胁全球水禽养殖产业,给养殖户造成巨大经济损失。目前,针对NDRV尚无商业化疫苗,传统疫苗平台存在免疫原性弱、安全性不足、储存条件苛刻等诸多局限,研发高效、安全、低成本的新型疫苗迫在眉睫。近日,由四川农业大学田斌副教授课题组开展的研究,在禽用新型疫苗研发领域取得重大突破——构建了基于壳聚糖寡糖-聚乙烯亚胺(CS-PEI)包裹环状RNA(circRNA)的纳米疫苗,该疫苗针对NDRV展现出优异的免疫保护效果,相关研究成果为禽用抗病毒疫苗的研发提供了全新思路和技术支撑,也进一步推动了环状RNA疫苗在兽医领域的应用进程。该研究以“CS-PEI包裹编码σC蛋白的circRNA纳米疫苗诱导鸭子对新型鸭呼肠孤病毒的保护性免疫”为核心,系统开展了从疫苗构建、递送系统优化到免疫 efficacy 验证的全链条研究,其严谨的实验设计、确凿的研究数据和突破性的研究结论,充分彰显了该成果的科学性和应用价值,为解决NDRV防控难题提供了切实可行的方案。
为何选择circRNA?新一代疫苗平台的独特优势
作为新一代核酸疫苗平台,环状RNA(circRNA)凭借其独特的共价闭合环状结构,从根本上克服了线性mRNA的不足。与线性RNA相比,circRNA无需5'帽结构和3'多聚腺苷酸尾,可有效抵抗核酸外切酶的降解,其半衰期是线性RNA的5倍以上,能够实现抗原的持续表达(通常超过7天);同时,circRNA通过内部核糖体进入位点(IRES)驱动帽非依赖翻译,可避免被模式识别受体识别,降低固有免疫激活和炎症因子释放,安全性更优;此外,circRNA还具有设计灵活、可实现多价抗原表达等特点,被认为是最具潜力的下一代疫苗平台之一。
此前,circRNA疫苗已在新冠病毒、狂犬病病毒、寨卡病毒等人类及动物病毒防控研究中展现出良好前景,但针对禽用病毒性疾病的circRNA疫苗研究仍处于空白阶段。该研究首次将circRNA疫苗平台应用于NDRV防控,填补了禽用circRNA疫苗的研究空白,具有重要的理论和实践意义。
核心突破:CS-PEI纳米递送系统,破解circRNA递送难题
核酸疫苗的高效递送是其发挥作用的关键,传统递送系统要么毒性较高,要么递送效率不足,且成本昂贵,难以满足兽医领域规模化应用需求。为解决这一难题,研究团队创新性地构建了基于天然生物大分子的CS-PEI纳米递送系统,将低分子量壳聚糖(30 kDa)与低分子量聚乙烯亚胺(1.8 kDa)偶联,形成兼具安全性和高效递送能力的纳米载体。
实验证实,该CS-PEI递送系统具有显著优势:其一,生物相容性极佳,在浓度高达80μM时仍对鸭胚成纤维细胞(DEF)无明显细胞毒性,远高于动物免疫所需浓度(50μM),确保了体内应用的安全性;其二,包裹效率高,在氮磷比(N/P)≥0.1时即可完全包裹circRNA,形成粒径约172.3 nm、zeta电位为+2.78 mV的球形纳米颗粒,该尺寸最适合细胞内吞作用,可有效促进circRNA进入靶细胞;其三,递送效率优异,在N/P=1时,其递送效率与商业化转染试剂Lipofectamine 2000相当,且能有效将circRNA递送至鸭子体内多个组织器官,为抗原持续表达提供了保障。与传统脂质纳米颗粒(LNPs)相比,CS-PEI递送系统具有制备简便、成本低廉、材料易获取等优势,更适合兽医领域规模化应用,为circRNA疫苗的产业化推广奠定了基础。
全面验证:疫苗免疫效果卓越,防护能力远超传统平台
研究团队以NDRV的σC蛋白为靶抗原——该蛋白是NDRV的主要结构蛋白和免疫原性蛋白,可介导病毒入侵宿主细胞,且能有效诱导机体产生特异性体液免疫和细胞免疫——构建了编码σC蛋白的circRNA(circRNA-σC),并与CS-PEI递送系统结合,形成CS-PEI-circRNA-σC纳米疫苗,通过多组实验全面验证其免疫效果。在体外实验中,研究团队证实,circRNA-σC可在DEF细胞和HEK293T细胞中高效表达σC蛋白,且表达持续时间长达7天,显著优于线性RNA-σC;CS-PEI纳米载体可有效保护circRNA不被降解,延长其在细胞内的半衰期,进一步提升抗原表达效率。在体内实验中,研究团队以3日龄雏鸭为研究对象,设计了多组免疫方案,全面评估疫苗的免疫原性和保护效果。此外,研究还证实,该疫苗可有效诱导雏鸭产生均衡的体液免疫和细胞免疫反应,通过持续表达抗原,模拟自然感染的免疫激活过程,从而形成长效免疫保护,为雏鸭早期免疫提供了理想方案。
前景展望:circRNA疫苗,开启兽医免疫防控新时代
随着核酸疫苗技术的不断发展,circRNA作为新一代疫苗平台,其应用前景日益广阔。结合该研究成果和当前circRNA疫苗的研究进展,未来circRNA疫苗在兽医领域的应用将呈现三大发展方向:一是多价疫苗研发。circRNA具有设计灵活的特点,可同时编码多种病毒的抗原蛋白,未来可构建针对禽流感、NDRV、鸭肝炎病毒等多种禽用病毒的多价circRNA疫苗,实现一针多防,降低免疫成本,提高免疫效率,为畜禽疫病的综合防控提供更便捷的方案:二是递送系统优化。虽然CS-PEI递送系统已展现出良好的应用潜力,但未来可通过表面修饰、靶向改造等方式,进一步提升其靶向性和递送效率;三是跨物种应用拓展。circRNA疫苗的核心优势具有通用性,未来可将该平台拓展至猪、牛、羊等其他畜禽,针对猪瘟、蓝耳病、牛病毒性腹泻等重大畜禽疫病,研发新型circRNA疫苗,推动兽医免疫防控体系的升级换代;此外,circRNA疫苗在 人畜共患病防控中也具有巨大潜力,可通过研发针对人畜共患病病毒的circRNA疫苗,实现畜禽疫病与人类健康的协同防控。此外,随着circRNA制备技术的不断优化,如提高环化效率、简化纯化工艺等,将进一步降低circRNA疫苗的研发和生产成本,推动其在兽医领域的规模化应用。该研究构建的CS-PEI-circRNA纳米疫苗平台,不仅为NDRV防控提供了新方案,更为整个禽用乃至兽用疫苗的研发开辟了新路径,有望开启兽医免疫防控的新时代。
总体而言,该研究成果是circRNA疫苗在禽用领域的一次重要突破,其严谨的实验设计、卓越的免疫效果和广阔的应用前景,充分彰显了我国在禽用新型疫苗研发领域的技术实力。相信在不久的将来,随着相关技术的不断完善,circRNA疫苗将成为畜禽疫病防控的重要力量,为我国乃至全球养殖业的健康发展提供有力保障。
四川农业大学动物医学院副教授田斌为论文第一作者,硕士研究生蔡倩迪和肖镇为并列一作,程安春教授为通讯作者,四川农业大学为第一通讯作者单位。本研究由成都市科学技术局项目(编号:2025-YF05-00721-SN)、国家自然科学基金项目(编号:32473042)、四川省自然科学基金项目(编号:2025ZNSFSC0210)以及四川农业大学自由探索专项基金项目(编号:2024ZYTS011 和 2521993028/2025)共同资助。
原文链接:https://doi.org/10.1016/j.ijbiomac.2026.151095