四川农业大学动物医学免疫学研究所在国际权威期刊《Nucleic Acids Research》发表遗传密码摆动识别的结构生物学基础
近日,四川农业大学动物医学院动物医学免疫学研究团队在核酸领域国际顶级学术期刊《Nucleic Acids Research》在线发表题为“Recognition of the wobble pair: quantum mechanical calculations of tRNA U34 or C34 modifications within the ribosomal decoding center”的研究论文。研究团队利用高分辨率的核糖体结构和量子力学计算,系统揭示了tRNA反密码子中第34位碱基的化学修饰如何调控非经典碱基配对,实现翻译过程中的“摆动识别”。这一成果为学界深入理解遗传密码的简并性、蛋白质翻译的精确性以及tRNA修饰的复杂生物学功能提供了新认知。
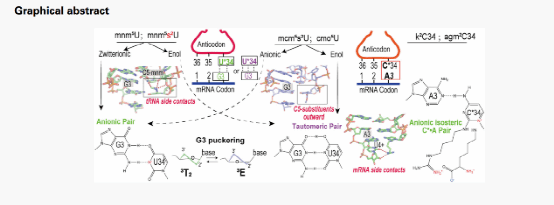
本研究聚焦于tRNA第34位高度保守的U34及C34修饰,围绕核糖体解码中心(Decoding Center)内关键的摆动碱基对展开了深入的系统分析。研究团队首先针对多种复杂的U34修饰(涵盖s⟡U、mnm⁵U、mcm⁵U、mnm⁵s⟡U及mcm⁵s⟡U)与密码子第三位G3形成的多种配对状态进行了热力学能量平衡计算。研究发现,碱基的化学修饰会显著改变其在阴离子形式与互变异构体之间的稳定性分布。计算数据显示,mnm⁵U·G和mnm⁵s⟡U·G配对能以稳定的阴离子/两性离子形式存在;而在涉及互变异构的构型中,mcm⁵s⟡U的烯醇式(Enol form)则表现出更强的热力学优势。
为进一步探究这些发现在生理环境下的意义,研究团队基于已解析的高分辨率核糖体结构,在真实的解码中心微环境模拟中对修饰碱基对进行了多维度分析。结果证实,第34位的化学修饰能够通过重塑氢键模式及局部空间位阻,预组织(Preorganize)出一种最适配于核糖体识别的摆动配对几何构象。这些修饰不仅精确调控了U34与G3之间的配对效能,还能在反密码子环的内部或外部诱导形成额外的氢键,从而锁定并稳定特定的识别构象。同时,研究还新发现了一种由密码子第三位核糖褶皱支持的柔性控制: G3核糖环微小的构象调整即可赋予碱基部分足够的自由度,使其能与多种修饰后的U34形成几何学上高度兼容的摆动配对。这些结构生物学证据与理论计算结果共同表明,tRNA第34位的化学修饰、碱基局部的电子云状态以及核糖体解码中心的微环境三者之间存在紧密的协同效应,共同构筑了摆动位点基于“几何互补”的摆动识别分子机制。
四川农业大学动物医学院动物医学免疫学研究所硕士研究生刘一为该论文的第一作者。四川农业大学欧旭敏讲师、法国科学院Eric Westhof院士以及贵州大学程安春教授为论文的共同通讯作者。该项研究工作得到了四川省科技厅项目及四川省兽药创新团队等项目的资助。
原文链接:https://academic.oup.com/nar/article/54/8/gkag299/8661662